小鼠常用给药方法
一、腹腔注射(Intraperitoneal Injection,IP)
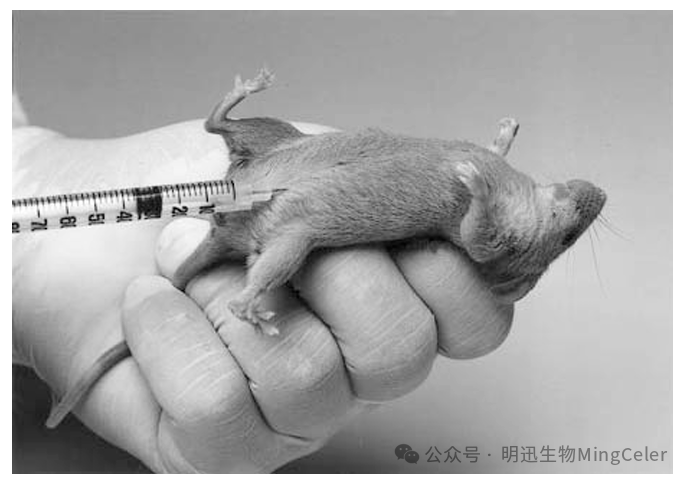
图源The Laboratory Mouse(Handbook of Experimental Animals)
操作步骤:
1.抓取小鼠:采用背侧保定法抓取小鼠,使其头部稍向后仰,腹部向上,小鼠左后肢用小指固定住。
2.消毒:用75%酒精棉球消毒注射部位,通常选择下腹部腹中线两侧0.5cm处(与大腿根部平齐)。
3.进针:将注射器针头刺入皮肤,进入皮下后,沿皮下向前推进23mm,针头与皮肤呈45度角刺入小鼠腹腔。穿透腹膜后,针尖的阻力会消失。
4.回抽与注射:回抽针栓,如无回血或液体即可注入药物。
5.拔针:注射完毕后,轻轻旋转针头,再缓慢拔出注射器,以免液体外漏。
注意事项:
1)注射位置需准确,避免伤及脏器。保定小鼠时使其头部稍向后仰,可使下腹部脏器上移。
2)进针角度向下45°,而非水平或向上,否则容易打到皮下形成鼓包。
3)注射前需用酒精棉球擦拭小鼠皮肤,注射后观察小鼠是否有异常反应。
二、灌胃给药(Intragastrical Gavage,IG)
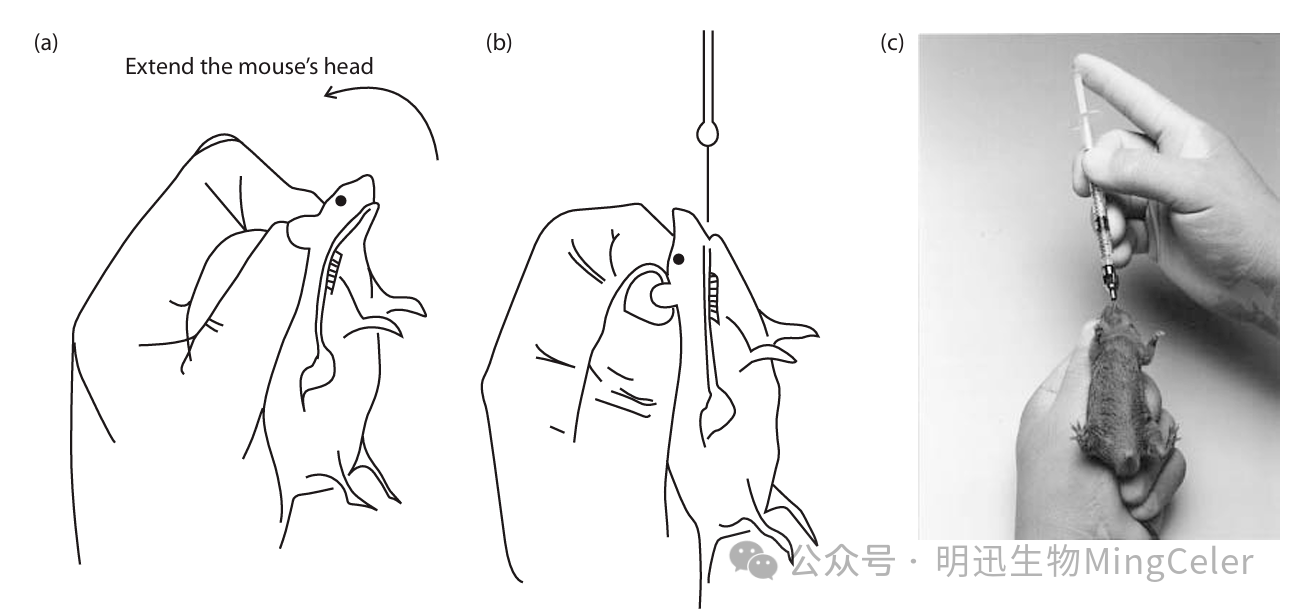
图源The Laboratory Mouse(Handbook of Experimental Animals)
操作步骤:
1.禁食:灌胃前将小鼠禁食48小时,避免胃内容物阻碍灌胃注射以及影响药物吸收速率。
2.固定小鼠:将小鼠固定成垂直体位,使其头、颈、身体成一条直线。右手拉住小鼠尾巴,左手的拇指、食指和中指揪住小鼠背部及颈部皮肤,小指和无名指压住小鼠的尾巴。
3.插针:右手持灌胃针,从一侧嘴角进针,轻压舌根,沿咽后壁徐徐插入食管。插入时应无阻力,若感到阻力或动物挣扎,应拔出重插。
4.注射药物:确认灌胃针位置无误后,缓慢注入药物。注射过程中观察小鼠是否有异常反应。
5.拔针:灌胃结束后轻柔地拔出灌胃针,观察是否有漏液并关注小鼠健康状态。
注意事项:
1)灌胃针的尖端有一个中空的金属球,目的是防止针头刺入气管或划伤消化道。
2)灌胃针插入深度需合适,一般插入小鼠34cm。
3)灌胃过程中要避免过快注射,以免引起小鼠呕吐。
三、皮下注射(Subcutaneous Injection,SQ)
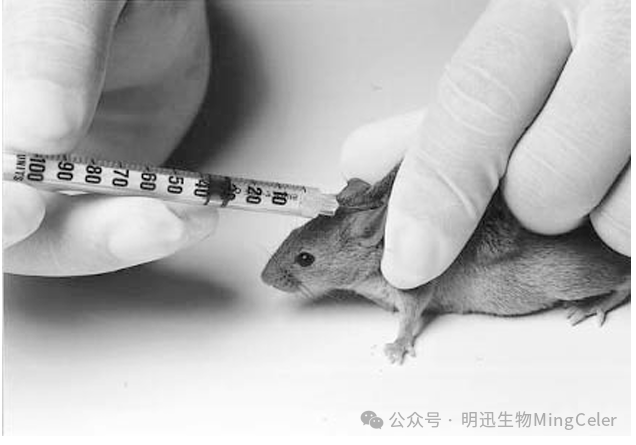
图源The Laboratory Mouse(Handbook of
Experimental Animals)
操作步骤:
1.固定小鼠:用左手拇指和食指捏起小鼠背颈部皮肤,使其皮肤绷紧。
2.消毒:用75%酒精棉球消毒注射部位。
3.进针:右手持注射器,针头斜面朝上,与皮肤呈45度角刺入皮下。刺入后针头轻轻左右摆动,易摆动说明已刺入皮下。
4.注射药物:回抽无血液后,缓慢推注药物。注射部位会出现一个小包。
5.拔针:注射完毕后,拔出针头,用无菌棉签轻压针孔片刻,防止药物外漏。
注意事项:
1)皮下注射的吸收速率较慢,适用于对组织无刺激性的药物。
2)注射部位可选择颈背部、腋下或大腿内侧的皮肤。
3)注射剂量需控制在小鼠0.10.3ml/10g,大鼠小于1ml/100g。
四、尾静脉注射(Intravenous Injection,IV)
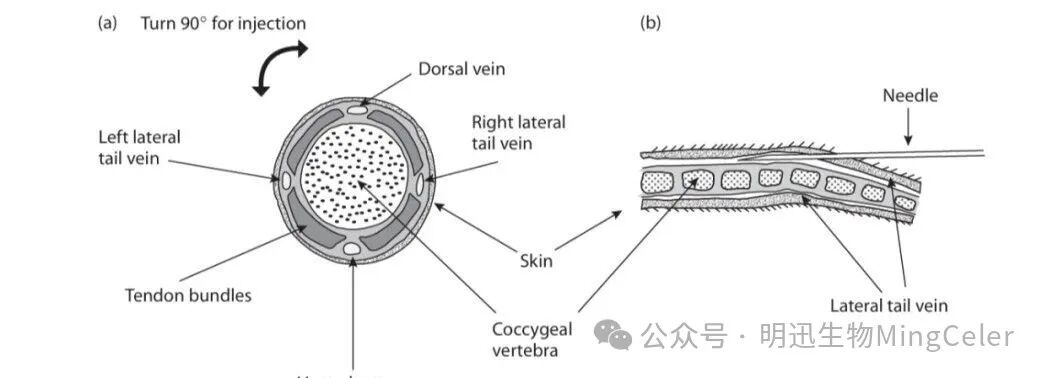

图源北京大学深圳研究生院实验动物中心
操作步骤:
1.固定小鼠:将小鼠放入固定器中,尾部自然外露。
2.准备血管:用4550℃的温水浸泡小鼠尾巴30秒,或用75%酒精棉球擦拭,使尾静脉充盈扩张。
3.进针:右手持注射器,针头斜面朝上,与尾部静脉平行,从尾部远端(尾尖方向)进针。针头刺入至少3mm后,轻推注射器,若无阻力,即可注射。
4.注射药物:缓慢注入药物,注射过程中观察小鼠是否有异常反应。
5.拔针:注射完毕后,用干棉球按压针孔片刻,防止出血。
注意事项:
1)小鼠尾部有三条静脉,两侧静脉较易固定,常用于注射。
2)注射时需避免刺入过深或刺破血管,导致药物外渗。
3)注射剂量一般为小鼠0.10.2ml/10g。
五、肌肉注射(Intramuscular Injection,IM)
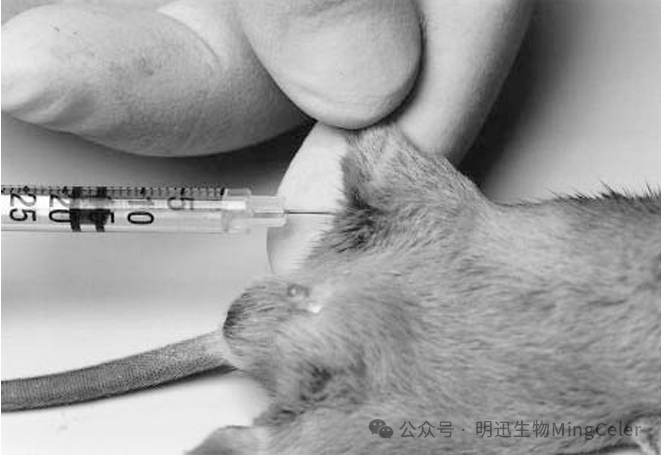
图源The Laboratory Mouse(Handbook of
Experimental Animals)
操作步骤:
1.固定小鼠:一般在动物麻醉后进行,或者由两个人配合操作,一人固定小鼠,一人注射。
2.选择注射部位:通常选择后肢大腿内侧或外侧的肌肉。
3.消毒:用75%酒精棉球消毒注射部位。
4.进针:左手固定后肢,右手持针垂直进针,回抽,看是否有液体回流。若无液回流,可继续注射,轻推药物,匀速注射。
注意事项:
1)肌肉注射药物水溶液时吸收迅速,适用于油溶液和某些刺激性物质。
2)注射完成后,用手轻轻按摩注射部位周围的肌肉组织,促进药液吸收。
六、皮内注射(Intradermal Injection,ID)
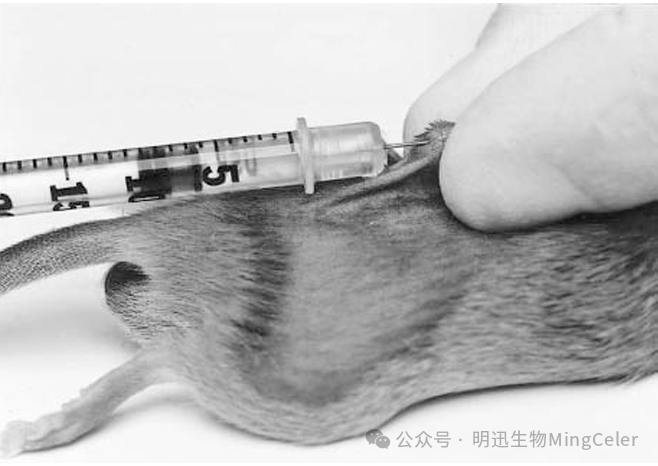
图源The Laboratory Mouse(Handbook of
Experimental Animals)
操作步骤:
1.固定小鼠:用左手将小鼠背部皮肤捏起,形成皱褶。
2.消毒:用70%酒精棉球消毒注射部位。
3.进针:右手持注射器,针头斜面朝上,与皮肤呈30°角刺入表皮与真皮之间,之后几乎和皮肤平行的方向在皮下走行35mm,再稍刺入,注射药物。
4.观察:注射后可见皮肤表面呈现小丘疹状隆起,并呈苍白色,一段时间后可消失。
注意事项:
1)一般选择小鼠背部脊柱两侧皮肤进行注射。
2)注射体积不要超过50ul,两点间隔1cm以上,避免产生组织坏死。
3)不要回抽注射器。
如何选择合适给药方式
1.根据实验目的选择
•研究口服生物利用度:选择灌胃给药。
•研究腹腔给药生物利用度:选择腹腔注射。
•研究药物的急性毒性:可选择尾静脉注射或腹腔注射。
2.考虑药物性质
•刺激性小的水溶性药物:适合腹腔注射。
•不溶于水的药物:可选择肌肉注射。
•需要快速起效的药物:可选择尾静脉注射。
3.考虑动物的健康状态
•幼鼠或体弱小鼠:避免使用肌肉注射,以免损伤肌肉组织。
•需要长期给药的实验:可选择皮下注射或灌胃给药。
4.考虑操作的可行性
•技术难度较高的给药方式:如尾静脉注射,需要一定的操作技巧和经验。
•操作简便的给药方式:如灌胃给药,较为易操作。
注:
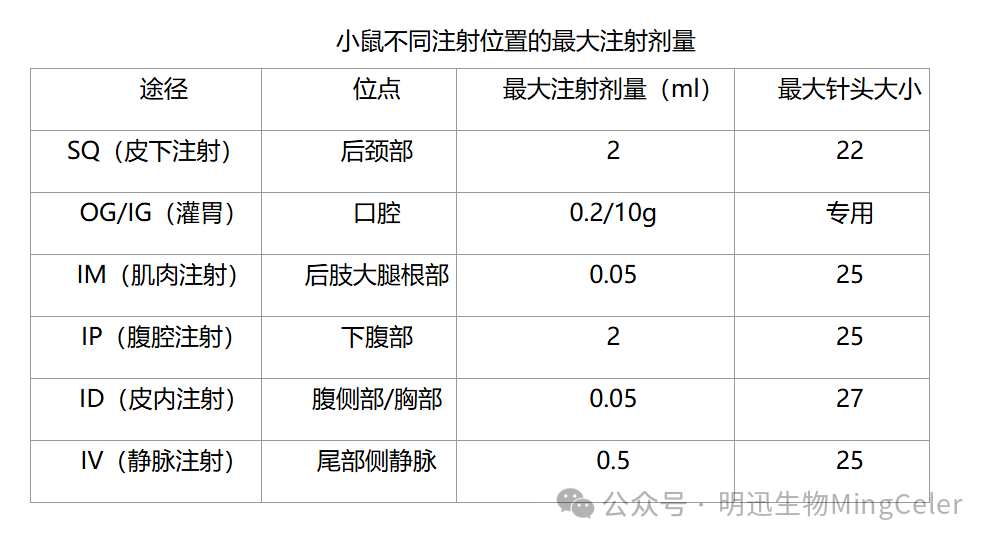
图源清华大学实验动物中心
明迅生物四倍体补偿技术
传统的动物模型技术包括原核显微注射技术和ES打靶嵌合技术,采用的是“小鼠造小鼠”模式,需要通过2-3代繁育过程获得纯合小鼠,整个过程至少耗时6-8个月乃至数年。
明迅生物自主研发的TurboMice™技术突破了小鼠造模周期长和复杂模型成功率低的技术难题,可实现几乎任何目标基因位点的编辑,从小鼠胚胎干细胞直接批量制备基因编辑目标小鼠,绕开常规技术耗时的繁育与筛选步骤,造模周期大大缩短,2-4个月内交付纯合子小鼠,欢迎各位老师咨询!
参考资料:
[1] https://www.larc.tsinghua.edu.cn/post/424
[2]南方医科大学爱课教学支持平台实验教学管理中心
[3]The Laboratory Mouse(Handbook of Experimental Animals)
[4]https://mp.weixin.qq.com/s/1O9Cjcw9DmhLrskxu0P6gQ
[5]https://mp.weixin.qq.com/s/audrVeCWsrszskJ4OQncDw
[6]https://mp.weixin.qq.com/s/jgqBZ_zw8QfQYwOVfU_Ifg
特别声明:本文来自明迅生物公众号,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在公众号后台留言联系我们。其他合作需求,请联系sales@mingceler.com。
免责声明:部分素材源于网络,如有侵权,联系删除,本文仅作信息交流之目的,文中观点不代表明迅生物立场,亦不代表明迅生物支持或反对文中观点。

 会员中心
会员中心 EN
EN

 2025.12.10.
2025.12.10.

