1、免疫缺陷小鼠的定义
免疫缺陷小鼠是指免疫功能缺陷的小鼠,由于先天性遗传或人工方法刻意造成,是进行现代医学研究的重要工具。其中人源化免疫缺陷小鼠是指带有人类功能性基因、细胞或组织的小鼠。
人源化小鼠模型的建立为人类疾病的研究提供了新的选择,其通常作为研究人类疾病的活体替代模型,在阐明发病机制、药物筛选等方面具有巨大的优势和广泛的应用前景。

2、免疫缺陷小鼠的发展
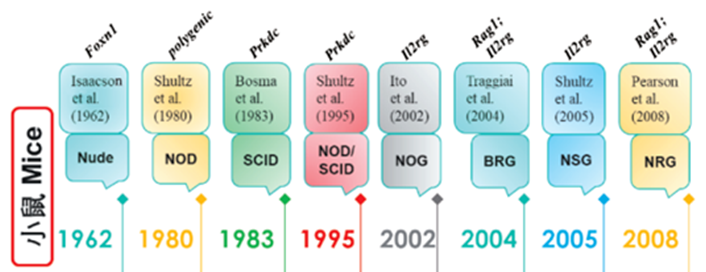
20世纪60年代第一次证实了Nude(Nude mouse)小鼠的免疫缺陷性,其是由于Foxn1基因突变引发胸腺上皮细胞发育异常,导致小鼠没有毛发和免疫力显著降低(血液中缺乏T细胞),但自然杀伤(natural killer, NK)细胞活性有所增强,且体液免疫能力正常,因此人类造血干细胞无法移植,这是此模型广泛应用的限制因素。
20世纪80年代,首次发现在CB17品系小鼠中可以植入人类外周血单个核细胞(Peripheral blood mononuclear cells, PBMCs),建立了CB17-SCID(Severe combined immunodeficiency)小鼠品系,它是人源化小鼠模型发展的第一阶段,但该品系由于缺失成熟的B、T细胞,且NK细胞活性和其固有的免疫力依然很高,使造血人类干细胞无法移植,因此,还是难以成为较好的人源化小鼠模型。
20世纪90年代,经过杂交产生的NOD(non-obese diabetic, NOD)-SCID品系小鼠可以更好地支持人类PBMCs或者造血干细胞的移植生长,且其伴随固有免疫系统缺陷和抑制NK细胞活性的现象,使得该品系成为近年来应用最广的SCID小鼠,它是人源化小鼠模型发展的第二阶段,但由于该品系小鼠生命周期短,且仍具有部分NK细胞活性,导致其作为人源化动物模型的广泛应用受限。
21世纪初叶,由白细胞介素2受体γ 链( interleukin 2 receptor gamma chain, IL-2Rγ)靶向突变形成的NOG和NSG小鼠品系是人源化小鼠模型发展的第三阶段,该品系小鼠的NK细胞、T细胞和B细胞的功能受到严重影响,使其更适于构建人源化小鼠模型,其应用领域包括肿瘤、血液系统疾病、感染性疾病等。
3、免疫缺陷小鼠的应用
免疫缺陷小鼠由于缺失正常的免疫功能,更容易感染疾病、形成肿瘤或在较高程度上接受外来移植物,因此,其是现代医学发展的重要工具。免疫缺陷小鼠的应用研究有以下几方面:
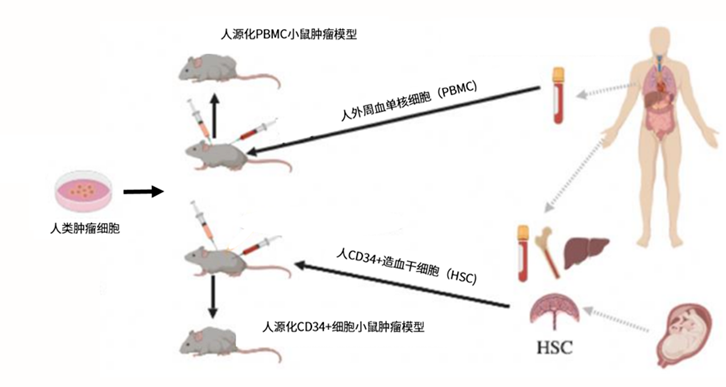
在肿瘤研究方面:通过在动物身上构建肿瘤模型,有利于科研人员探索肿瘤的发生机制,评价药物的药效及安全性,阐明药物的作用机制。不同背景的小鼠适用于不同的肿瘤研究:
BALB/c nude小鼠对移植入的人源肿瘤细胞或瘤块组织无排斥或排异反应,易成瘤,成功率高,实验成本较低,是目前使用最广泛的免疫缺陷小鼠模型;
SCID小鼠目前用于建立人源肿瘤模型,对于人员肿瘤细胞的移植成活率高于nude小鼠,且对恶性肿瘤的转移率高,适合探索肿瘤的转移和增殖情况;
NOD/SCID小鼠成瘤率高,可用于构建探索人NK细胞发育和功能的模型;
NOG、NSG、NCG及NPG小鼠成瘤率高,适于建立人源肿瘤异种移植、重建人免疫系统及研究肿瘤的免疫治疗或化疗药物的免疫反应等。
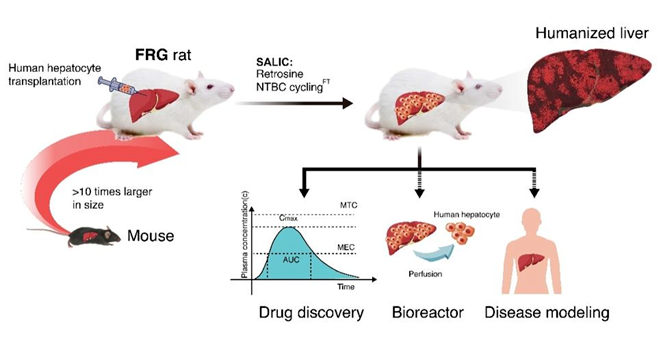
在感染性疾病研究方面:感染性疾病是由病原微生物感染所致,但许多遗传病,如:获得性免疫缺陷综合征、疟疾、丝虫病等的病原体并不感染小鼠等动物,因此限制了通过动物模型进行活体研究,人源化小鼠模型的出现为研究这类疾病及开展疫苗测试提供了一个有效平台。通过将人造血祖细胞和(或)外周血细胞悬浮液(带有支持人免疫细胞生长的血细胞周围组织)移植入免疫缺陷小鼠可获得人类免疫系统(Human immune system, HIS)小鼠,该小鼠作为唯一可被人类免疫缺陷病毒(Human immunodeficiency virus, HIV)感染的动物模型,可用于测试抗病毒化合物。由于小鼠免疫系统可以抵抗肝炎病毒的侵袭,大多数小鼠不能表现感染性肝脏疾病,因此限制了传统人源化肝鼠嵌合模型的发展,AFC8小鼠模型具有功能性人类免疫系统,在注射了从人类胎肝组织提取的CD34+HSC及肝起源细胞(hepatic progenitor cells, Hep)后,即形成AFC8-hu HSC/Hep小鼠模型,该模型最大的优势是小鼠肝脏可以受丙型肝炎病毒感染及产生抗丙型肝炎病毒的T细胞反应,因此其是一种非常好的研究乙肝、丙肝病毒体内感染最终导致肝纤维化全过程的模型。
在白血病研究方面:由于在免疫缺陷小鼠-人类白血病模型中白血病细胞的增殖和分化受到如同骨髓微环境一样的调控,因此为研究白血病增殖、分化及其调控机制提供了独特的条件。免疫缺陷小鼠模型还可以检测白血病细胞生长和散播的能力,评价某些已知在体外能杀伤或致白血病细胞凋亡的药物,成为判断患者预后以及探索新的白血病治疗手段的重要方法之一。
在痛风研究方面:痛风是一种常见的代谢性疾病,是尿酸钠晶体在关节内及其周围组织广泛沉积所引起的急慢性非感染性炎性反应。由于人类基因在进化过程中基因突变,导致了尿酸氧化酶基因失活,这也是人类易患痛风的重要原因。而包括小鼠在内的实验动物,尿酸代谢主要依赖体内的尿酸氧化酶,因此人类和小鼠在尿酸代谢和排泄上明显不同,利用普通小鼠模型所得到的实验结论与人体实际情况存在差异,有资料显示,尿酸氧化酶基因剔除后,小鼠可出现高尿酸血症和痛风症状,成为与人类痛风发病机制非常相似的自发性高尿酸血症和痛风小鼠动物模型,把人的关节滑膜植入剔除尿酸氧化酶基因的SCID小鼠背部,并向该小鼠体内注入人的免疫细胞将成为更符合人类痛风发病特点的人源化小鼠模型。痛风人源化小鼠模型在开展痛风发病机制研究及药物筛选方面具有广阔的应用前景。
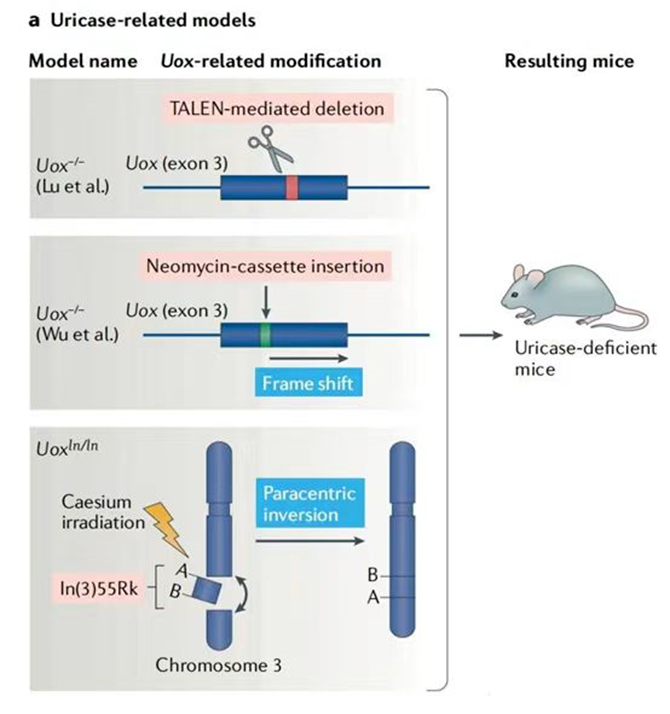
QuickMice™ nuNPG重度免疫缺陷小鼠
品系名称:NOD-PKDCtm1Ming-IL2rgtm1Ming/MCL
品系描述:
nuNPG品系是一个近交系NOD遗传背景上建立的重度免疫缺陷小鼠模型,具有Prkdctm1Ming和IL2rgtm1Ming基因的突变。
Prkdctm1Ming是通过敲除Prkdc外显子阻断T和B细胞的发育并诱导免疫缺陷。与SCID小鼠来源的PrkdcSCID天然突变相比,Prkdctm1Ming没有PrkdcSCID突变随小鼠年龄增长出现少量Prkdc泄漏表达而导致免疫系统少量恢复的缺点。IL2rgtm1Ming突变是编码细胞因子受体共有亚基γ的基因IL2rg的KO突变,IL2rg也称为白细胞介素-2受体亚基γ,是白介素(IL-2、IL-4、IL-7、IL-9和IL-15)所共有的受体亚基。该基因对许多造血细胞的分化和功能是必要的,对自然杀伤细胞(NK)的发育至关重要。在NOD近交系小鼠上, Prkdctm1Ming和IL2rgtm1Ming突变组合诱导了T、B和NK淋巴细胞谱系缺乏的严重免疫缺陷。
明迅生物于2023年通过同源重组对Prkdc和IL2rg完全KO突变而获得了nuNPG品系(NOD-PKDCtm1Ming-IL2rgtm1Ming/MC)。nuNPG小鼠具有纯合突变Prkdctm1Ming和IL2rgtm1Ming的近交系遗传背景。nuNPG小鼠的表型已根据MINGCELER GENETIC POLICY®进行了验证。
品系优势:
·迄今世界上免疫缺陷程度高的工具小鼠;
·外显子删除后没有Prkdc残留表达;
·少量细胞即可成瘤,依赖于细胞系或细胞类型;
·无B淋巴细胞泄漏;
应用领域:
·人源细胞或组织移植
·肿瘤和肿瘤干细胞研究
·ES和iPS细胞研究
·造血和免疫学研究
·人类疾病感染模型研究
·新的人源化动物模型研发
验证数据:
1、nuNPG小鼠外周血中T/B/NK细胞检测利用流式细胞术(Flow Cytometry)对 nuNPG 免疫缺陷小鼠及野生型对照小鼠外周血单个核细胞(PBMCs)进行检测,通过特 异性标记 T 细胞(CD3+)、B 细胞(CD19+)及自然杀伤细胞(NK 细胞,NK1.1)。数据表明,nuNPG 小鼠模型具备高度免疫缺陷特性,可有效消除内源性 T/B/NK 细胞对实验的干扰,为肿瘤移植、 免疫重建及人源化细胞治疗等研究提供理想的免疫缺陷背景。
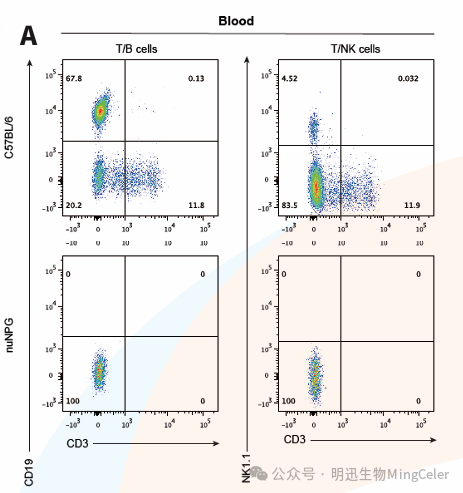
nuNPG免疫缺陷小鼠外周血免疫细胞耗竭特征分析。结果显示:nuNPG小鼠外周血中T/B/NK三类免疫细胞几乎完全缺失,而野生型小鼠呈现正常免疫细胞分布。
2、nuNPG小鼠成瘤性检测
通过NPG小鼠皮下构建人肝癌细胞SMMC7721、HepG2肿瘤模 型,检测NPG小鼠成瘤效率。实验证明该模型可高效、稳定地用于肝癌相关药物筛选及肿瘤生物学研究。
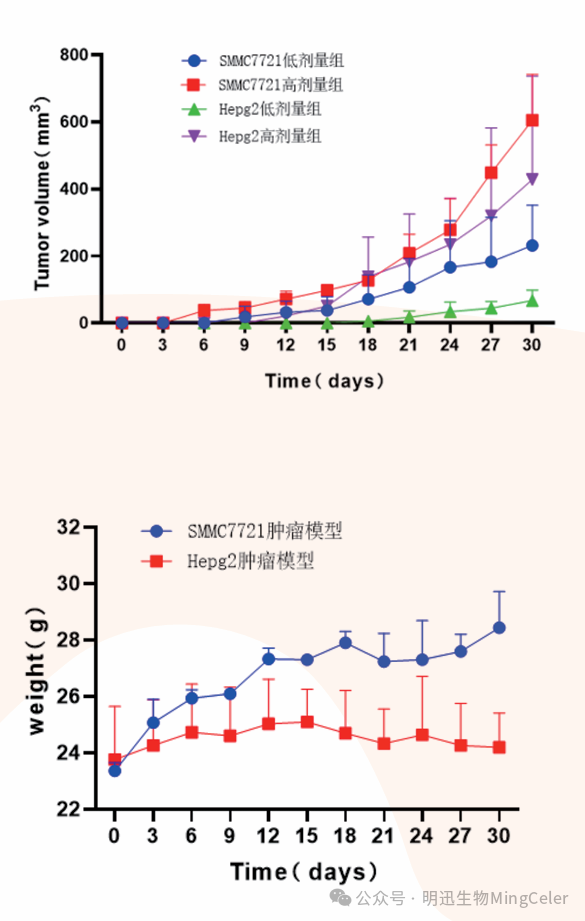
肿瘤体积随时间和接种细胞剂量变化,成瘤率达100%。 各组动物体重稳定,显示了良好的耐受性。

动物肿瘤解剖图:肿瘤体积与肿瘤细胞接种数量成正比
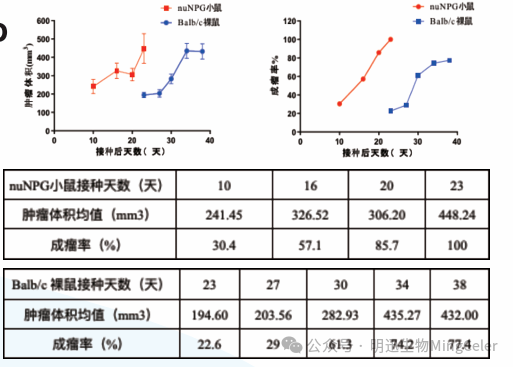
对比nuNPG小鼠和Balb/c裸鼠的LnCap CDX模型的生长曲线和成瘤率:从结果来看,nuNPG小鼠的成瘤所需时间更短,肿瘤生长速度更快。在接种第23天时nuNPG小鼠成瘤率就达到100%,而Balb/c裸鼠接种第23天成瘤率只有22.6%。
参考文献:
[1]孔维波,徐静雯. 免疫缺陷小鼠模型在肿瘤治疗研究中的应用[J]. 今日药学,2023,33(3):186-190. DOI:10.12048/j.issn.1674-229X.2023.03.005.
[2]安凌波,张茂森,栾晶. 人源化小鼠模型的研究进展[J]. 中国免疫学杂志,2022,38(22):2809-2816,封3-封4. DOI:10.3969/j.issn.1000-484X.2022.22.022.
[3]张茹君, 李东明. 免疫缺陷小鼠模型研究进展[J]. 医药卫生: 临床研究, 2017, (2): 56-57.
特别声明:本文来自明迅生物公众号,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在公众号后台留言联系我们。其他合作需求,请联系sales@mingceler.com。
免责声明:部分素材源于网络,如有侵权,联系删除,本文仅作信息交流之目的,文中观点不代表明迅生物立场,亦不代表明迅生物支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗指导,请前往正规医院就诊。

 会员中心
会员中心 EN
EN

 2025.12.15.
2025.12.15.

