实验室新引进小鼠,如何鉴定小鼠的基因型?常用的小鼠基因型鉴定方法有常规PCR鉴定,qPCR鉴定及测序。下面一起来详细聊聊吧~
除了实验室新引入小鼠外,还有以下几种情况需要进行基因型鉴定:
1、繁殖配对前:在进行小鼠繁育时,对繁育对进行基因型鉴定可以保证亲本的基因型准确无误。这样可以有效避免因亲本基因型错误而导致子代基因型混乱,从而提高繁育效率和实验结果的可靠性。
2、子代小鼠:如果亲本产生的后代有多种基因型(例如杂合子配杂合子),就需要对子代小鼠进行基因型鉴定。通过鉴定,可以筛选出符合实验要求的特定基因型小鼠,确保实验的顺利进行。
01、常用鉴定方法
1)常规PCR鉴定
目前最常用的基因型鉴定方法。通过设计特异性引物,利用PCR技术扩增目标基因片段,然后通过琼脂糖凝胶电泳分析PCR产物的条带差异来判断小鼠的基因型。
特点:常用于肿瘤学、免疫学及炎症研究。操作简便、成本较低,适用于大多数实验室。
2)qPCR鉴定
qPCR(实时荧光定量PCR)是一种更为精确的基因型鉴定方法。它通过荧光信号实时监测PCR扩增过程,不仅可以判断基因型,还可以定量分析基因表达水平。
特点:灵敏度高、特异性强,但对设备和技术要求较高。
3)测序
对于一些复杂的基因型鉴定,如点突变小鼠,测序是必不可少的手段。通过测序可以直接读取目标基因的碱基序列,从而准确判断基因型。
特点:测序成本较高,但其结果最为准确可靠。
02、PCR鉴定操作步骤
一. 样本采集:
常用的样本来源包括小鼠的尾尖、耳廓、脚趾等组织。
一般建议在小鼠出生后9-14天进行采样。采样后,样本可置于-20°C冰箱保存备用。
二. 提取DNA模板:
2.1 试剂
a、鼠尾裂解液

图源清华大学实验动物中心
b、 蛋白酶K溶液
蛋白酶K(简称PK, 20mg/ml in MilliQ),stored @-20℃
c、TE Buffer

图源清华大学实验动物中心
2.2 实验流程
1) 每个样品加入300ul裂解液+5ul PK(20mg/ml),55°C消化过夜(不少于4h)。
2) 乙醇沉淀:加入600ul(双倍体积)-20℃预冷的无水乙醇,上下颠倒,直到可以清楚的看见絮状沉淀。
3) 离心12000rpm,5min。
4) 晾干:离心后,倒出上层液体。倒放在一张平板纸上(注意一定要立着,这样里面的液体采用较快的流到EP管口)。差不多5-10min左右,把立着的管子换一个位置,轻轻向下按一下(目的是用平板纸吸去聚集在管口的液体,此步可以节省很多晾干时间)。等待30-60min至完全晾干,此时沉淀变透明,提取的DNA质量佳。
5) 加入200ul MilliQ水或TE溶液,使用上下振摇的方式充分溶解DNA。
6) 取3ul gDNA模板,在25ul的反应体系中进行PCR。
三. PCR:
3.1 反应体系(25ul体系)

图源清华大学实验动物中心
3.2 反应条件(touchdown)
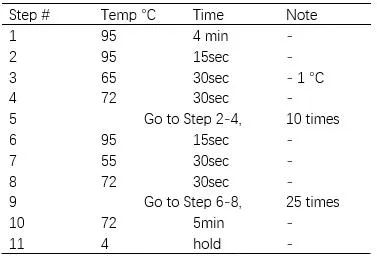
图源清华大学实验动物中心
四. 电泳
4.1 配置凝胶:根据目标条带配置1-3%的琼脂糖凝胶,将1g-3g琼脂糖溶于100ml TAE缓冲液,微波炉加热至琼脂糖融化,加入10ul核酸染料(EB替代物),倒入电泳模板中,并插入梳子,待冷凝后使用。
4.2 加样:向琼脂糖凝胶中加入适量的DNA,小孔建议加10ul,大孔建议加20ul,并根据目标条带大小选择合适DNA marker加入凝胶中。
4.3 跑胶:电泳仪设置120V电压,跑20-30min。
4.4 成像:使用凝胶成像系统观察、拍摄照片。
4.5 编辑胶图,出基因型鉴定结果报告。
03、注意事项
1)对照设置:在基因型鉴定实验中,设置合适的对照组非常重要。通常需要设置以下几种对照:
野生型对照:用于判断基因型及PCR体系是否合适。
空白对照:不含有任何组织/DNA的对照组,用来质控PCR体系是否发生污染。
内部阳性对照:引物通常扩增与目的基因无关的基因组DNA区域,用来判断PCR体系和模板质量是否合适。
2)引物设计:引物设计是PCR成功的关键。
设计引物时需要注意引物的GC含量、二级结构、二聚体、退火温度、长度、特异性等方面的问题。如果引物设计不佳,可能会导致PCR产物少或没有目的条带。
3)污染控制:在实验过程中,要严格控制污染。样本采集时要避免交叉污染,DNA提取和PCR操作要在无菌环境下进行,使用一次性耗材和无核酸酶污染的试剂。
04、常见问题及解决方法
1)PCR产物少或没有目的条带
可能的原因包括:组织提取物中的污染物抑制了PCR反应、组织消化不够充分、引物设计不佳、待扩增片段GC含量偏高或长度较长等。
解决方法:检测抑制物、延长消化时间、优化引物设计、使用适合高GC含量或长片段扩增的试剂和条件。
2)出现非特异性条带
可能是因为退火温度不合适、引物二聚体或模板量过多。解决方法:优化退火温度、减少模板量。
3)条带弥散
可能是由于DNA模板降解或PCR反应条件不佳。
解决方法:优化DNA提取方法,避免DNA降解;调整PCR反应条件,如变性时间、退火温度等。
参考资料:
[1]https://mp.weixin.qq.com/s/6J0hPRiS6H6tIs1st2bFBw
[2]王廷华.PCR理论与技术(第三版).科学出版社,2005.
特别声明:本文来自明迅生物公众号,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在公众号后台留言联系我们。其他合作需求,请联系sales@mingceler.com。
免责声明:部分素材源于网络,如有侵权,联系删除,本文仅作信息交流之目的,文中观点不代表明迅生物立场,亦不代表明迅生物支持或反对文中观点。

 会员中心
会员中心 EN
EN

 2025.02.25.
2025.02.25.

