什么是多发性硬化?
多发性硬化(multiple sclerosis,MS)是一种以中枢神经系统(CNS)多发性炎症脱髓鞘、轴突变性及胶质瘢痕形成为核心病理特征的慢性免疫介导性疾病,临床表现为认知减退、疲劳、肌无力、感觉异常、共济失调及进行性神经功能残疾。全球患者约280万,好发于20-40岁青壮年,是青壮年非创伤性神经功能障碍的首要病因。
按自然病程可划分为复发-缓解型(RRMS,80%)、继发进展型(SPMS)、原发进展型(PPMS,10%~15%)及进展复发型(PRMS,<5%)四种表型。
发病机制
多发性硬化(MS)的发病遵循外周启动-中枢持续的经典模式。其起始源于遗传易感个体在环境因素(如EB病毒感染)触发下,免疫耐受被打破。这导致外周的髓鞘反应性CD4⁺ T细胞(主要为Th1和Th17亚群)被异常激活。
这些细胞随后上调趋化因子受体(如CCR6、CXCR3),并通过其表面黏附分子(如LFA-1)与血脑屏障(BBB)内皮细胞上的配体(如ICAM-1、VCAM-1)相互作用,同时释放基质金属蛋白酶(如MMP-9)降解细胞外基质,从而突破BBB,侵入中枢神经系统(CNS)。进入CNS后,活化的T细胞与局部的抗原提呈细胞(如被激活的小胶质细胞和浸润的巨噬细胞)相遇,发生二次致敏,急剧放大炎症级联反应。
CD4⁺ T细胞释放大量肿瘤坏死因子-α(TNF-α)和干扰素-γ(IFN-γ)等促炎因子。其中,TNF-α通过激活其受体下游的NF-κB等信号通路,不仅直接诱导少突胶质细胞凋亡和髓鞘损伤,还进一步破坏BBB完整性,形成恶性循环。同时,被激活的CD8⁺ 细胞毒性T细胞通过释放穿孔素(Prf1)和颗粒酶,直接杀伤表达髓鞘抗原的少突胶质细胞。
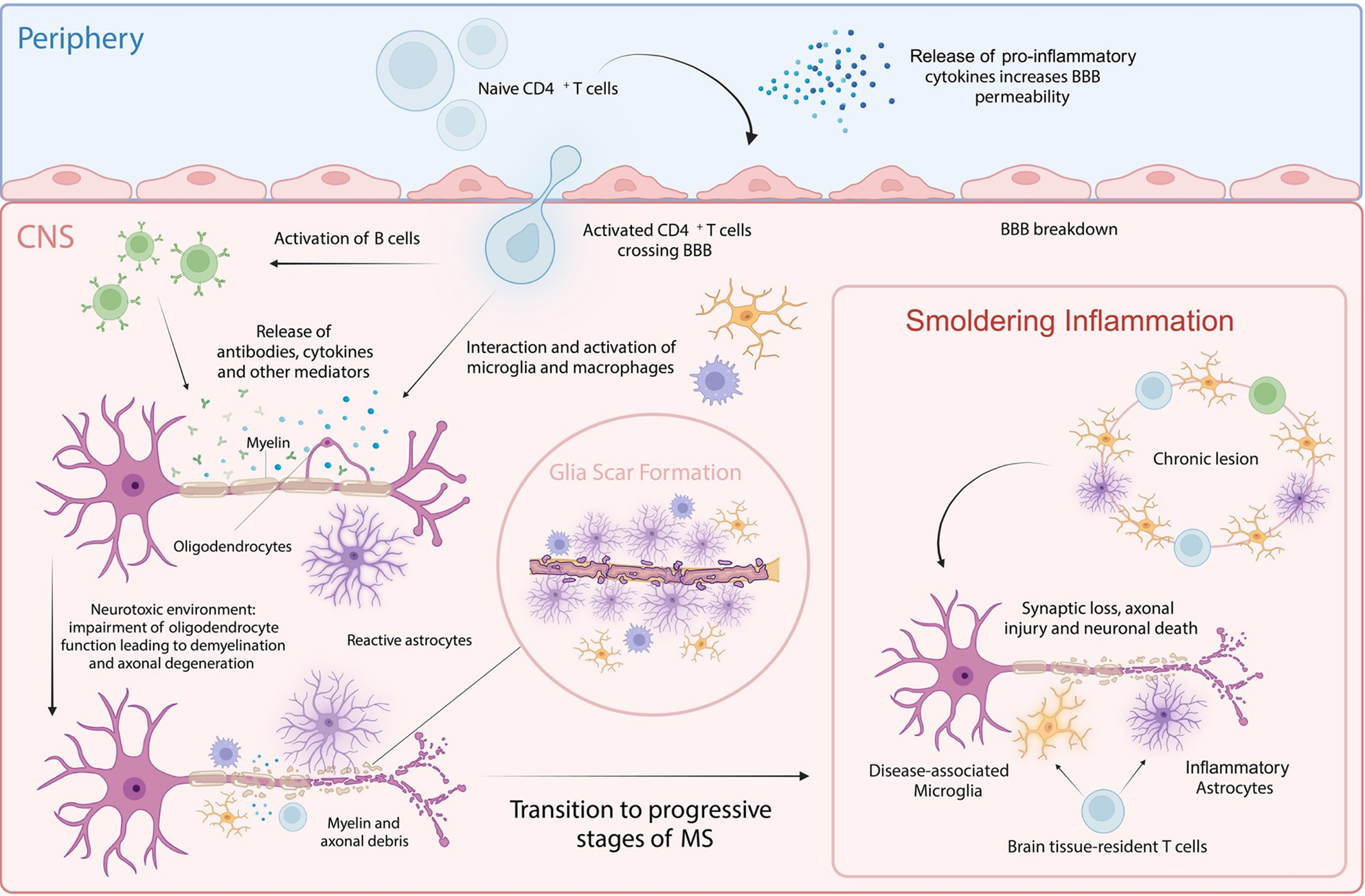
图源Brain organoid methodologies to explore mechanisms of disease in progressive multiple sclerosis
在慢性炎症环境下,小胶质细胞通过TREM2-DAP12、CX3CR1等信号通路被持续异常激活,极化为促炎的M1表型或疾病相关表型(DAM),其PI3K-Akt/mTOR等代谢通路发生紊乱。这导致小胶质细胞持续释放TNF-α、IL-1β、活性氧(ROS)等神经毒性物质,并产生GM-CSF等细胞因子进一步招募外周免疫细胞,共同营造并维持一个强大的抑制性炎症微环境,严重阻碍由少突胶质前体细胞分化为成熟细胞所介导的再髓鞘化修复过程,更直接导致线粒体功能障碍和慢性的轴突变性与损伤。最终不可逆的轴突丢失和神经元死亡成为神经功能永久性缺损的基础,并驱动疾病从复发缓解型(RRMS)向继发进展型(SPMS)或原发进展型(PPMS)过渡。
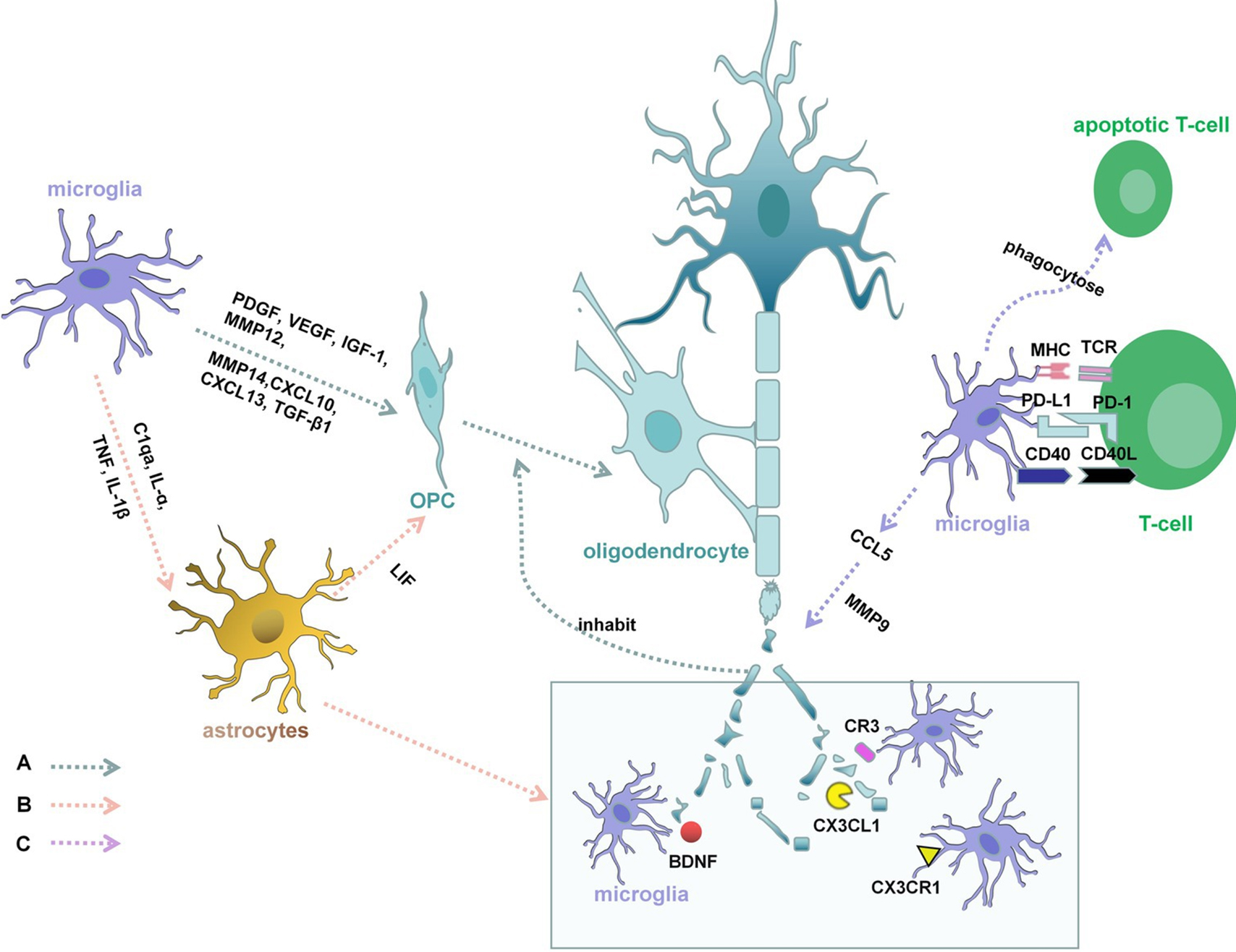
图源Microglia in the context of multiple sclerosis
基因治疗
基因编辑技术:特异性敲除自体T细胞中编码髓鞘反应性T细胞受体的基因序列或关键共刺激分子基因。经体外扩增后回输的基因编辑T细胞可显著降低其自身反应性,实现抗原特异性免疫耐受的诱导。
腺相关病毒(AAV)载体治疗:AAV载体中枢递送抗炎细胞因子(IL-10、TGF-β1)或再髓鞘化因子(LINGO-1-Fc、BMP4),在EAE中已证实可减轻脱髓鞘并促进少突胶质前体细胞(OPC)分化。
小鼠模型
Prf1-KO小鼠:敲除穿孔素基因Prf1,其表现出显著减轻的临床症状,中枢神经系统内炎症浸润、脱髓鞘及轴索损伤均大幅减少。
TNF-α-KO小鼠:敲除肿瘤坏死因子TNF-α,其中枢神经系统内炎症反应减弱,血脑屏障破坏减轻,脱髓鞘和少突胶质细胞丢失减少。
IL-23p19-KO小鼠:敲除IL-23的特异性亚基p19,其致病性Th17细胞反应被显著削弱,EAE发病率降低、发病延迟且严重程度减轻,中枢神经系统内炎性细胞募集减少。
CX3CR1-GFP小鼠:通过在小胶质细胞特异性表达的Cx3cr1基因位点敲入绿色荧光蛋白基因,可直观地观察小胶质细胞在健康、炎症(如EAE)及神经退行过程中的形态动态、分布迁移以及与周围神经元、突触的相互作用。
明迅生物助力基因治疗
基因治疗为罕见病带来了希望,但其研发和验证离不开动物模型的支持。明迅生物借助自主研发的TurboMice™技术已研发了多个罕见病小鼠模型,TurboMice™技术突破了小鼠造模周期长和复杂模型成功率低的技术难题,可实现几乎任何目标基因位点的编辑,可短至2个月由胚胎干细胞直接制备完整纯合基因编辑小鼠模型。
明迅生物可根据客户需求定制各类MS小鼠模型,如Prf1-KO小鼠、TNF-α-KO小鼠、IL-23p19-KO小鼠、CX3CR1-GFP小鼠等,欢迎各位老师来咨询。
参考资料:
[1]王茜, 陆正齐, 李蕊. 多发性硬化的治疗进展[J]. 重庆医科大学学报, 2024, 49(5): 597-600. DOI:10.13406/j.cnki.cyxb.003500
[2]Patil, M.S.; Lin, L.Y.; Marsh-Wakefield, F.; James, E.J.; Palendira, M.; Hawke, S.; Grau, G.E. Multiple Sclerosis: Immune Cells, Histopathology, and Therapeutics. Sclerosis 2024, 2, 117-139. https://doi.org/10.3390/sclerosis2030009
[3] Zhang X, Chen F, Sun M, Wu N, Liu B, Yi X, Ge R, Fan X. Microglia in the context of multiple sclerosis. Frontiers in Neurology. 2023 Jun 9;14:1157287. doi:10.3389/fneur.2023.1157287.
[4]Simões-Abade MBC, Patterer M, Nicaise AM, Pluchino S. Brain organoid methodologies to explore mechanisms of disease in progressive multiple sclerosis. Frontiers in Neurology. 2023;14:1157287. doi:10.3389/fneur.2023.1157287.
特别声明:本文来自明迅生物公众号,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在公众号后台留言联系我们。其他合作需求,请联系sales@mingceler.com。
免责声明:部分素材源于网络,如有侵权,联系删除,本文仅作信息交流之目的,亦不是提供治疗方案,文中观点不代表明迅生物立场,亦不代表明迅生物支持或反对文中观点。

 会员中心
会员中心 EN
EN

 2025.12.17.
2025.12.17.

